Dalam ilmu kimia, reaksi reduksi ester atau reduksi Bouveault–Blanc merupakan salah satu reaksi penting yang mengubah ester menjadi alkohol. Reaksi ini terjadi dengan bantuan zat pereduksi, seperti lithium aluminium hydride (LiAlH₄) atau sodium borohydride (NaBH₄), di bawah kondisi tertentu.
Reduksi Bouveault–Blanc ini sangat berbeda dari reaksi esterifikasi. Jika esterifikasi melibatkan pembentukan ester dari asam karboksilat dan alkohol melalui proses kondensasi, maka reduksi ester adalah kebalikannya, yakni memutuskan ikatan ester untuk menghasilkan alkohol sebagai produk utamanya.
Baca Juga: Contoh Makromolekul Organik dan Peran Pentingnya dalam Kehidupan
Proses ini biasanya berfungsi dalam sintesis organik untuk menghasilkan alkohol primer dari ester dengan efisiensi tinggi.
Reaksi Reduksi Ester, Apa Bedanya dengan Reaksi Esterifikasi?
Dalam kimia, reaksi esterifikasi berbeda dengan reduksi Bouveault–Blanc, meskipun keduanya melibatkan senyawa ester. Perbedaan utama terletak pada fungsi dan hasil perubahan struktur kimia dari masing-masing reaksi.
Reduksi Bouveault–Blanc adalah proses di mana ester berubah menjadi alkohol. Reaksi ini melibatkan penambahan hidrogen (H₂) atau agen pereduksi lain seperti Lithium Aluminium Hydride (LiAlH₄) atau Natrium Borohidride (NaBH₄).
Agen pereduksi tersebut mampu mengurangi ikatan rangkap karbon-oksigen (C=O) dalam gugus karbonil ester, menghasilkan alkohol. Tujuan utama reaksi ini adalah untuk mengonversi ester menjadi alkohol.
Di sisi lain, reaksi esterifikasi merupakan proses pembentukan ester melalui reaksi antara alkohol dan asam karboksilat, atau kadang dengan jenis asam lain. Reaksi ini bertujuan menghasilkan ester dari kombinasi asam dan alkohol.
Secara singkat, reduksi ester berfokus pada pembentukan alkohol dari ester, sedangkan esterifikasi bertujuan membentuk ester dari alkohol dan asam.
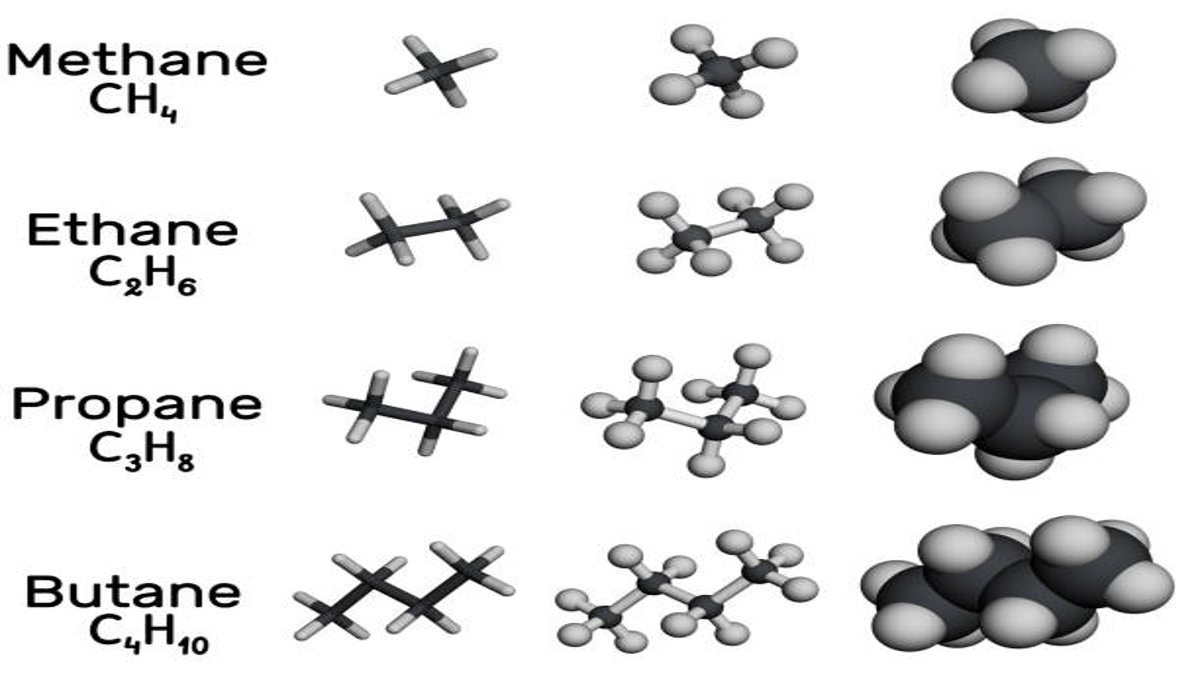
Kimia Ester
Ester terkenal memiliki aroma yang menyenangkan, sehingga banyak digunakan dalam produk sehari-hari seperti sabun, makanan, dan parfum. Kehadirannya menjadi salah satu fungsi organik yang fundamental dalam memahami kimia di kehidupan sehari-hari.
Dengan memahami ester, kita juga dapat menggali lebih dalam tentang berbagai aspek kimia organik lainnya. Dalam reaksi reduksi ester, senyawa ini memegang peranan penting karena menjadi komponen utama dalam proses tersebut.
Pemahaman yang mendalam tentang ester mencakup karakteristiknya, baik sifat kimia maupun fisikanya, metode sintesis, serta bentuk kemunculannya. Selain itu, penghargaan terhadap kompleksitas dan keragaman kimia organik yang terkait dengan ester juga menjadi bagian penting dari kajian ini.
Reaksi Utama Ester
Hidrolisis ester adalah reaksi kimia di mana ester terurai menjadi asam karboksilat dan alkohol dengan adanya air serta katalis berupa asam atau basa. Sementara itu, saponifikasi ester merupakan proses di mana ester bereaksi dengan basa kuat.
Menghasilkan garam asam karboksilat (sabun) dan alkohol. Selain itu, reaksi reduksi ester adalah proses di mana ester direduksi menjadi alkohol primer dengan bantuan agen pereduksi yang kuat.
Contoh dan Kasus
Dalam pembahasan ini, terdapat contoh reduksi ester, yaitu reduksi metil metanoat (HCOOCH₃) menggunakan gas hidrogen (H₂) dengan katalis nikel (Ni). Proses ini menghasilkan metanol (CH₃OH), di mana ester mengalami reduksi menjadi alkohol primer.
Baca Juga: Pengertian dan Reaksi Oksidasi Alkohol
Reaksi kimia ester, seperti hidrolisis, saponifikasi, dan reduksi, memungkinkan kita memperoleh berbagai produk kimia yang sangat bermanfaat untuk kehidupan sehari-hari.
Mekanisme yang Melibatkan Radikal Bebas
Ester merupakan turunan asam karboksilat yang berasal dari menggantikan gugus -OH dari asam karboksilat dengan gugus -OR. Reaksi reduksi ester sering melibatkan mekanisme radikal bebas.
Radikal bebas sendiri adalah atom atau molekul dengan elektron yang tidak berpasangan pada lapisan terluarnya. Reaksi radikal bebas biasanya terdiri dari tiga tahapan utama, yaitu inisiasi, propagasi, dan terminasi.
Reduksi ester dapat kita lakukan melalui hidrogenasi katalitik menggunakan gas hidrogen, katalisator, panas, dan tekanan, atau dengan mereaksikan ester dengan litium aluminium hidrida (LiAlH₄), yang kemudian berlanjut ke proses hidrolisis untuk menghasilkan alkohol primer.
Selain itu, reduksi ester dengan mekanisme radikal bebas juga dapat kita lakukan menggunakan logam natrium (Na). Logam natrium bertindak sebagai reduktor berelektron tunggal, yang mentransfer satu elektron.
Dalam proses ini, butuh empat atom natrium untuk sepenuhnya mereduksi ester menjadi alkohol. Etanol berfungsi sebagai sumber proton dalam reaksi ini, sehingga mendukung proses reduksi ester menjadi alkohol primer melalui mekanisme yang melibatkan reaksi radikal bebas.
Tidak Pakai Metanol
Dalam mekanisme reduksi ester, metanol tidak berfungsi sebagai sumber proton. Metanol, yang merupakan alkohol, umumnya berperan sebagai pelarut atau sumber proton dalam reaksi esterifikasi dan reaksi asam-basa.
Namun, pada reduksi ester, proton yang dibutuhkan berasal dari agen pereduksi yang lebih efektif, seperti gas hidrogen (H₂) atau senyawa pereduksi kuat seperti litium aluminium hidrida (LiAlH₄).
Baca Juga: Ikatan Kimia Glukosa yang Jadi Sumber Energi Bagi Organisme
Metanol tidak cukup kuat untuk mendonorkan proton yang berperan dalam memutus ikatan ganda karbon-oksigen (C=O) pada gugus karbonil ester selama reaksi reduksi ester. Oleh karena itu, reduksi ester mengandalkan sumber proton yang lebih reaktif untuk menghasilkan alkohol primer secara efisien. (R10/HR-Online)

 1 month ago
33
1 month ago
33